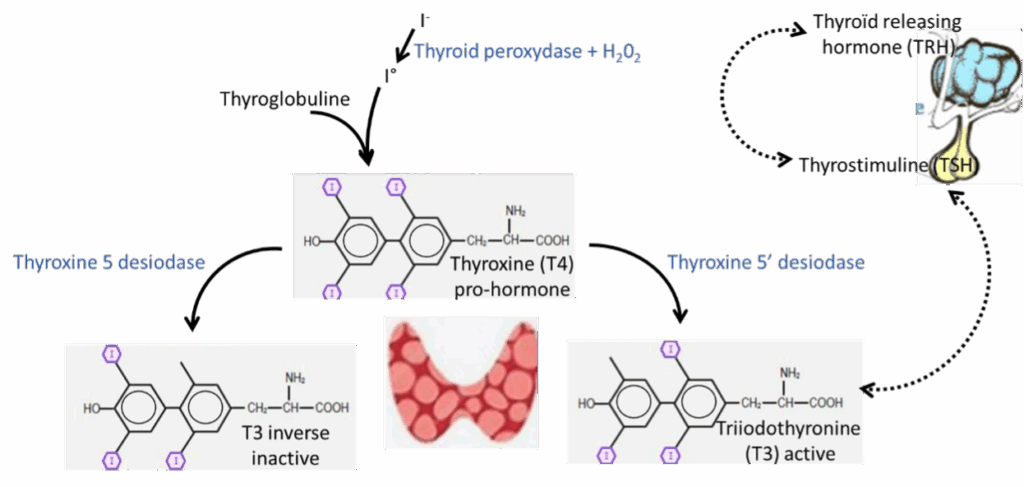
Carence
Si les carences sévères en iode sont devenues rares, les carences légères sont très fréquentes y compris en Europe. Les effets sur la thyroïde sont fonction de la durée et de la sévérité de la carence. Les populations les plus à risque sont les femmes en âge de procréer et les végans.
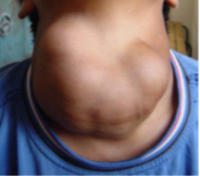
Goitre d’après Zimmerman 2009
Une déficience en iode est associée à une hyperstimulation de la thyroïde. La TSH augmente et, si elle perdure, la T3 baisse, la thyroïde devient hypertrophique et est associée à un stress oxydant. La rupture de la balance redox augmente le risque de cancer, de nodules thyroïdiens, de goitre multi-nodulaires chez l’adulte et le sujet âgé. Les nodules hyperactifs sont fréquemment responsables d’hyperthyroïdie.
Certains aliments, en bloquant la fixation de l’iode dans la thyroïde (légumes de la famille des choux, manioc, soja, arachide, patates douces…) peuvent conduire à une carence en iode si consommés en quantité. D’autres facteurs tels que le tabagisme, la grossesse et les variations saisonnières peuvent aggraver le risque de carence.
Chez la femme enceinte, la carence en iode augmente la Tg ; peut entrainer une hypertension gestationnelle, des avortements, des malformations fœtales, une augmentation de la mortalité périnatale.
Si non traitée, elle provoque chez l’enfant
- une hypotonie ;
- un sommeil excessif ;
- un retard du développement psychomoteur : déficit intellectuel précoce, retard aux apprentissage, diminution sévère du quotient intellectuel (crétinisme), retard de croissance qui aboutit à un nanisme disharmonieux ;
- une peau jaunâtre ;
- de la constipation ;
- un goitre.
Le traitement doit être commencé le plus tôt possible pour éviter les effets délétères irréversibles et permettre une croissance et un développement intellectuel pratiquement normal.
Chez l’adulte, l’hypothyroïdie par carence en iode se manifeste, en autre, par :
- une fatigue chronique, apathie, somnolence
- une sensibilité au froid augmentée,
- une prise de poids,
- un rythme cardiaque anormalement lent,
- des cheveux et une peau sèche,
- une concentration élevée de cholestérol sanguin,
- des crampes et douleurs musculaires,
- de la constipation,
- des règles irrégulières et une infertilité,
La carence en iode augmente la fréquence des troubles thyroïdiens évitables, tels que nodules thyroïdiens, goitre multi nodulaires et hyperthyroïdie, notamment chez les adultes et les sujets âgés. La TSH est abaissée et la T3 augmentée. Non traitée, elle entraine des troubles du rythme cardiaque, un risque accru d’infarctus du myocarde, de troubles cognitifs, d’ostéoporose et une sarcopénie.
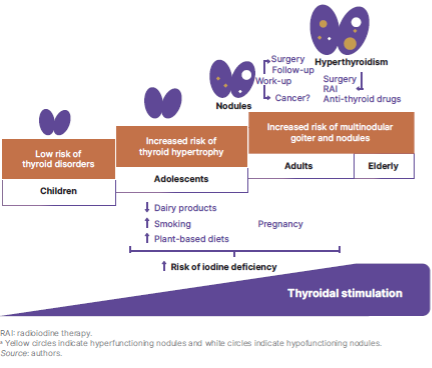
Effets de la carence en iode peu sévère en fonction de l’âge, OMS 2024